القلويات الترابية
تشكل المعادن القلوية الترابية alkaline earth metals الفصيلة الثانية أو (IIA) في الجدول الدوري. وهي البريليوم[ر] Be، والمغنزيوم[ر] Mg والكلسيوم Ca، والسترنسيوم Sr والباريوم Ba والراديوم[ر] Ra. ويطلق عليها اسم القلوية الترابية لأن المشتغلين قديماً بالكيمياء كانوا يطلقون اسم تراب على المواد غير المعدنية التي لاتنحل بالماء ولاتتأثر بالنار، ولأن »أتربة« هذه العناصر مثل الكلس الحي CaO والمغنيزيا MgO تعطي تفاعلاً قلوياً.
أهم مميزات هذه الفصيلة خواصها المعدنية، وقوتها الإرجاعية، وتشكيلها مركبات تأخذ فيها درجة الأكسدة +2. كما أن كثيراً من هذه المركبات ضعيف الانحلال في الماء. وتعد هذه العناصر بالمقارنة مع عناصر الفصيلة الأولى أضعف من حيث الصفات المعدنية وقوة الإرجاع.
تحوي المعادن القلوية الترابية إلكترونين s، في حين تكون طبقتها التالية مماثلة للطبقة الإلكترونية الخارجية للغاز الخامل الذي يسبق المعدن في الجدول الدوري.
x4Be :[He] 2s2
x12Mg :[Ne] 3s2
x20Ca :[Ar] 4s2
x38Sr :[Kr] 5s2
x56Ba :[Xe] 6s2
x88Ra :[Rn] 7s2
وكما في حالة المعادن القلوية فإن ذرات المعادن القلوية الترابية تفقد إلكترونيها بسهولة ولكن بدرجة أقل، كما أنها لاتميل إلى الاتحاد بإلكترونات إضافية، لذا فإن المعادن القلوية الترابية تتصف بخواص كيمياوية معدنية نموذجية أيضاً. وتزداد هذه الخواص شدة من البريليوم حتى الراديوم. وتكون هذه الخواص ضعيفة نسبياً في حالة البريليوم الذي يشبه الألمنيوم في كثير من الخواص فيلازمه في معظم فلزاته، وهو مثله معدن مذبذب. كما أن المغنزيوم يشبه بخواصه الزنك، خاصة بسهولة انحلال كبريتاته بخلاف كبريتات الكلسيوم والسترونسيوم والباريوم. وتؤلف هذه العناصر الثلاثة الأخيرة فئة المعادن القلوية الترابية بالمفهوم الضيق لهذه التسمية التي أُطلقت عليها لتشابه خواص ماءاتها مع خواص ماءات المعادن القلوية.
وبصورة عامة يمكن تعليل تناقص الخاصة القلوية وتعاظم الخاصة الحمضية عند الانتقال من فئة المعادن القلوية إلى المعادن القلوية الترابية بتناقص أنصاف أقطار الذرات والشوارد.
إن العنصر الأخير في هذه الفصيلة هو الراديوم عنصر مشع نادر. وهو معدن قلوي ترابي بخواصه العامة، وينتج من تفكك العناصر الأثقل منه وخصوصاً اليورانيوم؛ ولذلك يصادف مع خامات اليورانيوم خاصة البتش بلند (pitch blend U3O8 غير النقي) ويعد الخام الحاوي على 0.25غ من الراديوم في الطن من الخامات الغنية.
وجودها في الطبيعة ـ استحصالها ـ خواصها الفيزيائية ـ استعمالاتها
المغنزيوم والكلسيوم المعدنان الوحيدان بين المعادن القلوية الترابية اللذان ينتشران انتشاراً واسعاً في القشرة الأرضية، فتبلغ النسبة الوزنية المئوية للمغنيزيوم 2.35%. وتوجد أملاحه في مياه المحيطات أيضاً. كما تبلغ النسبة المئوية للكلسيوم في القشرة الأرضية 25.3% وزناً. أما في حالة السترنسيوم والباريوم فتساوي هذه النسبة 0.35% و0.05% بالترتيب، وتوجد هذه العناصر الثلاثة الأخيرة في الطبيعة بشكل كربونات وكبريتات خاصة.
وكان الإنكليزي السير همفري ديڤي (1778ـ1829) Sir Humphry Davy أول من عزل المغنزيوم بطريقة التحليل الكهربائي بكميات صغيرة وأطلق عليه اسم مغْنيوم magnium وذلك حتى لايحصل التباس بينه وبين المنغنيز، إلا أن اسمه بقي مغنزيوم. كما عزل ديڤي الكلسيوم والسترنسيوم والباريوم بالطريقة نفسها عام 1808.
يحصل على عناصر هذه الفصيلة بالحالة المعدنية الحرة بتحليل أملاحها المصهورة تحليلاً كهربائياً.
وتتصف المعادن القلوية الترابية بلون أبيض فضي، وهي أكثر قساوة من المعادن القلوية. فالباريوم وهو أقل المعادن القلوية الترابية قساوة يتميز بقساوة معدن الرصاص. كما أن درجات انصهار المعادن القلوية الترابية أعلى من درجات انصهار المعادن القلوية.
ويبين الجدول (1) بعض الثوابت الفيزيائية لعناصر الكلسيوم والسترنسيوم والباريوم. ويلاحظ من هذا الجدول أن كهرجابية المعادن القلوية الترابية تماثل تقريباً كهرجابية المعادن القلوية، ويلاحظ أن تغير الكمون النظامي يتفق مع تغير طاقة التشرد.
أما من حيث استعمالات عناصر هذه الفصيلة فإن المغنزيوم هو المعدن الوحيد الذي يستعمل بالحالة الحرة بصورة واسعة لتحضير المواد النارية بسبب الضوء الشديد المتولد عن احتراقه، ويدخل البريليوم والمغنزيوم والكلسيوم مع المعادن الأخرى في تركيب كثير من الخلائط المعدنية فتكسبها قساوة عظيمة.
وتستعمل مركبات عناصر هذه الفصيلة في الصناعة، خاصة مركبات الكلسيوم والمغنزيوم في صناعة الإسمنت والزجاج وبعض المواد الأخرى كالأميانت والتلك. وللمغنزيوم أهمية خاصة في التحضيرات العضوية (تفاعل غرينيار).
الصفات الكيمياوية للكلسيوم والسترنسيوم والباريوم
تتصف عناصر هذه الفصيلة بكهرجابية عالية وبنشاط كيمياوي كبير كالمعادن القلوية. فمن الناحية المبدئية تفكك هذه العناصر الماء والحموض بانطلاق الهدروجين، وتشكل مركبات شاردية مع العناصر الكهرسلبية مع ازدياد بروز هذه الخواص عند الانتقال من البريليوم حتى الباريوم ومن العناصر الأقل كهرسلبية إلى العناصر الأكثر كهرسلبية.
أهم المركبات
ـ الهاليدات: تنتج من التفاعل مع الهالوجينات مركبات بلورية لا لون لها صيغتها العامة MX2 تتبلور مع الماء فتضم 6جزيئات في حالة الكلسيوم والسترنسيوم (MX2.6H2O) وجزيئين في حالة الباريوم. كما تكون هذه البلورات جيدة الانحلال في الماء، ويستثنى من ذلك الفلوريدات التي تكون صعبة الانحلال، ولاتشكل بلورات مميهة بصورة عامة.
أهم الهاليدات من الوجهة العملية كلوريد الكلسيوم: ويستعمل كلوريد الكلسيوم اللامائي مجفِّفاً، كما أن محاليله المائية تستعمل في المختبرات حمامات مائية ذات درجات غليان أو درجات تجمد مختلفة حسب تركيز الكلوريد. فتتدرج درجة الغليان من 101 ْس حتى 178 ْس وتتدرج درجة التجمد من -0.05 ْس حتى -51 ْس.
ـ الأكاسيد والماءات: يتم تفاعل المعادن القلوية الترابية مع الأكسجين في الدرجة العادية من الحرارة فتتغطى هذه المعادن في الهواء بطبقة من الأكسيد MO. غير أن هذه الطبقة تكون كتيمة في حالة المغنزيوم فتمنع استمرار التفاعل. وينشط التفاعل بشدة بتسخين المعدن ويتشكل إضافة إلى الأكسيد MO النتريد M3N2 وفوق الأكسيد MO2 في حالة Ba¨Sr¨Ca.
وتتصف الأكاسيد MO بخواص أساسية باستثناء أكسيد البريليوم الذي يتميز بخواص أساسية وحمضية (أكسيد مذبذب).
والأكاسيد MO مواد بيضاء صعبة الانصهار تتفاعل مع الماء مشكلة الماءات M(OH)2. وتزداد درجة انحلال الماءات وتشردها في الماء عند الانتقال من البريليوم حتى الباريوم، فتكون ماءات البريلوم ماءات مذبذية، في حين تكون ماءات المغنزيوم أساساً متوسط القوة، وماءات الباريوم أساساً قوياً نوعاً ما. أكسيد الكلسيوم وهو الكلس الحي ذو استعمالات معروفة.
ـ فوق الأكاسيد والأكاسيد العليا: تشكل المعادن القلوية الترابية مثل المعادن القلوية فوق أكاسيد وأكاسيد عليا. ويحصل على فوق الأكاسيد MO2 إما بالطريقة الرطبة بتفاعل الماء الأكسجيني H2O2 مع ماءات المعدن، وهو تفاعل تعديل حمض (H2O2) بأساس، كما في حالة الكلسيوم إذ يحصل على فوق أكسيده بالتفاعل:
وإما بالطريقة الجافة بتسخين أكسيد المعدن في الهواء أو في جو من الأكسجين حتى درجة حرارة معينة، كما في حالة الباريوم إذ يحصل على فوق أكسيده BaO2 بتسخين الأكسيد العادي وهو بشكل كتلة مسامية حتى درجة 500 ْس في تيار من الهواء.
وتكون فوق الأكاسيد مواد بيضاء، تحوي في بنيتها الشاردة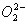 وتعطي بتفاعلها مع الحموض الماء الأكسجيني والملح الموافق للمعدن. أهمها من الوجهة التطبيقية فوق أكسيد الباريوم الذي يستخدم صناعياً للحصول على الماء الأكسجيني بتفاعله مع حمض الكبريت وفق المعادلة:
وتعطي بتفاعلها مع الحموض الماء الأكسجيني والملح الموافق للمعدن. أهمها من الوجهة التطبيقية فوق أكسيد الباريوم الذي يستخدم صناعياً للحصول على الماء الأكسجيني بتفاعله مع حمض الكبريت وفق المعادلة:
ـ النتريدات: يتفاعل الآزوت بالتسخين عند درجة عالية من الحرارة فتتشكل النتريدات M3N2. وتعد هذه المركبات مشتقة من غاز النشادر. وهي مواد قاسية ذات درجات انصهار عالية تتفكك بالماء أو بالحموض مشكلة النشادر.
ـ الكربيدات: لايتم تفاعل المعادن القلوية الترابية مع الكربون سوى في درجة عالية من الحرارة أيضاً وتتشكل الكربيدات. وهي تتصف بصورة عامة ببنية شاردية خاصة في حالة الكلسيوم والسترنسيوم والباريوم التي تعطي الكربيد MC2
الذي يحوي الشاردة الخطية السالبة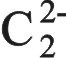 .
.
أهم الكربيدات كربيد الكلسيوم الذي يعرف في التجارة باسم الكربيد، ويستعمل لتوليد غاز الأستيلين
ـ الهدريدات: لتفاعل المعادن القلوية الترابية مع الهدروجين يجب التسخين إلى درجة عالية من الحرارة أيضاً وتتشكل الهدريدات. وهي مواد بيضاء ذات بنية بلورية شاردية تحترق في الهواء بمجرد تسخينها متحولة إلى الأكسيد MO وماء. فهي مواد مرجعة قوية تفكك الماء وفق المعادلة:
التفاعل مع الماء والحموض: إن المعادن القلوية الترابية تزيح مبدئياً الهدروجين من مركباته كالماء والحموض والكحولات. وفي الواقع تفكك هذه المعادن الماء مع ازدياد نشاط التفاعل من البريليوم حتى الباريوم وفق المعادلة:
غير أن طبقة الأكسيد أو الماءات المتشكلة تعيق استمرار التفاعل خاصة في حالة البريليوم والمغنزيوم والكلسيوم بسبب بطء انحلال نواتج التفاعل. وبالتسخين ينشط التفاعل. ويحدث تفاعل مماثل مع الكحولات بانطلاق الهدروجين أيضاً كالتفاعل مع الكحول الإيتيلي:
أما مع الحموض فيتم التفاعل بقوة، وتزداد شدة التفاعل دوماً من البريليوم حتى الباريوم وتتشكل أملاح الشوارد M2+. وتتشكل هذه الأملاح أيضاً بتفاعل الحموض مع أكاسيد أو ماءات هذه العناصر أيضاً.
شوارد المعادن القلوية الترابية لا لون لها، وأملاحها لا لون لها أيضاً بصورة عامة. منها ما ينحل جيداً في الماء كأملاح الشوارد: ومنها ما يكون صعب الانحلال لا في الماء فحسب، بل في المحلات الأخرى، كأملاح الشوارد
ومنها ما يكون صعب الانحلال لا في الماء فحسب، بل في المحلات الأخرى، كأملاح الشوارد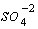 و
و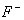 و
و و
و و
و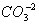 . ولكثير من هذه الأملاح تطبيقات مهمة في الصناعة وسيكتفى بدارسة بعض هذه الأملاح كالكبريتات والنترات والكربونات.
. ولكثير من هذه الأملاح تطبيقات مهمة في الصناعة وسيكتفى بدارسة بعض هذه الأملاح كالكبريتات والنترات والكربونات.
الكبريتات MSO4: تتبلور كبريتات المغنزيوم والكلسيوم مع عدد مختلف من جزيئات الماء فتكون صيغها:
BeSO4. 4H2O¨CaSO4. 2H2O¨MgSO4. 7H2O
أما كبريتات السترنسيوم والباريوم فلا تحوي بلوراتها ماء تبلور. وتتناقص درجة الانحلال في الماء عند الانتقال من البريليوم حتى الباريوم. فكبريتات البريليوم والمغنزيوم جيدة الانحلال، أما كبريتات الباريوم فهي ملح صعب الانحلال. ويقل الانحلال بارتفاع درجة الحرارة.
وأهم أملاح الكبريتات كبريتات الباريوم المستعملة في الطب، وكبريتات الكلسيوم التي تتبلور في الدرجة العادية من الحرارة مع جزيئي ماء، وتشكل ما يعرف باسم «الجبصين». إذا سخنت هذه الكبريتات إلى درجة 150 ْس فقدت قسماً من مائها وتحولت إلى 2CaSO4.H2O. وعند مزج هذه المادة الأخيرة بالماء تتحد مرة أخرى مع الماء لتكوين البلورات المميهة مما يؤدي إلى تصلب المزيج مع ازدياد حجمه، ويستفاد من ذلك لصب القوالب كما هو معروف.
النترات M(NO3)2: تتبلور نترات المعادن القلوية الترابية مع عدد من جزيئات الماء باستثناء نترات الباريوم، وصيغها:
Mg(NO3)2.6H2O, Ca(NO3)2.4H2O, Sr(NO3)2.4H2O
وهي تنحل جيداً في الماء باستثناء نترات الباريوم أيضاً التي تكون متوسطة الانحلال. تتفكك النترات بالتسخين فاقدة في مرحلة أولى ماء التبلور ومن ثم تتحول إلى أكاسيد الآزوت والأكاسيد MO وأكسجين.
الكربونات MCO3: الكربونات المعتدلة MCO3 عديمة الانحلال في الماء. وهي تتفكك بالتسخين حيث ينطلق CO2 ويتشكل الأكسيد MO. وتترسب الكربونات بإضافة مزيد من الشوارد
إلى محلول يحوي الشوارد M2+x.
وأهم الكربونات ـ من الناحية العملية ـ كربونات الكلسيوم. وتستخدم بمختلف أشكالها الطبيعية (الأحجار الكلسية) للحصول على الكلس والإسمنت وفي صناعة الزجاج.
فالإسمنت مزيج من مختلف سيلكات وألومينات الكلسيوم وبالدرجة الأولى المركبات: Ca2SiO5, Ca2SiO4, Ca3(AlO3)2. فيعد الإسمنت ناتج اتحاد مختلف الأكاسيد الآتية بنسب مختلفة: CaO, SiO2, Al2O3, Fe2O3 حيث يقوم الأكسيد CaO بدور الأكسيد الأساسي في حين تقوم الأكاسيد الأخرى بدور الأكاسيد الحمضية.
وتتفاعل الكربونات MCO3 مع ثنائي أكسيد الكربون المنحل في الماء مكونة الكربونات الحمضية M(HCO3)2 الأكثر انحلالاً من الكربونات، أهمها كربونات الكلسيوم الحمضية Ca(HCO3)2.
يسبب وجود أملاح الكلسيوم في الماء قساوته. وتكون هذه القساوة مؤقتة عندما يحوي الماء الكربونات الحمضية Ca(HCO3)2 وذلك لسهولة إزالة هذه القساوة بترسيب الكلسيوم بشكل CaCO3 بغلي الماء إذ تتفكك الكربونات الحمضية إلى كربونات معتدلة و CO2. وتكون القساوة دائمة عندما يكون الملح المنحل CaSO4 أو CaCl2. وتُزال هذه القساوة إما بإضافة Na2CO3 لترسيب CaCO3، وإما بالتبادل الشاردي الذي يخلص الماء من شوارد الكلسيوم، وإما بالتقطير.
غدير زيزفون
تشكل المعادن القلوية الترابية alkaline earth metals الفصيلة الثانية أو (IIA) في الجدول الدوري. وهي البريليوم[ر] Be، والمغنزيوم[ر] Mg والكلسيوم Ca، والسترنسيوم Sr والباريوم Ba والراديوم[ر] Ra. ويطلق عليها اسم القلوية الترابية لأن المشتغلين قديماً بالكيمياء كانوا يطلقون اسم تراب على المواد غير المعدنية التي لاتنحل بالماء ولاتتأثر بالنار، ولأن »أتربة« هذه العناصر مثل الكلس الحي CaO والمغنيزيا MgO تعطي تفاعلاً قلوياً.
أهم مميزات هذه الفصيلة خواصها المعدنية، وقوتها الإرجاعية، وتشكيلها مركبات تأخذ فيها درجة الأكسدة +2. كما أن كثيراً من هذه المركبات ضعيف الانحلال في الماء. وتعد هذه العناصر بالمقارنة مع عناصر الفصيلة الأولى أضعف من حيث الصفات المعدنية وقوة الإرجاع.
تحوي المعادن القلوية الترابية إلكترونين s، في حين تكون طبقتها التالية مماثلة للطبقة الإلكترونية الخارجية للغاز الخامل الذي يسبق المعدن في الجدول الدوري.
x4Be :[He] 2s2
x12Mg :[Ne] 3s2
x20Ca :[Ar] 4s2
x38Sr :[Kr] 5s2
x56Ba :[Xe] 6s2
x88Ra :[Rn] 7s2
وكما في حالة المعادن القلوية فإن ذرات المعادن القلوية الترابية تفقد إلكترونيها بسهولة ولكن بدرجة أقل، كما أنها لاتميل إلى الاتحاد بإلكترونات إضافية، لذا فإن المعادن القلوية الترابية تتصف بخواص كيمياوية معدنية نموذجية أيضاً. وتزداد هذه الخواص شدة من البريليوم حتى الراديوم. وتكون هذه الخواص ضعيفة نسبياً في حالة البريليوم الذي يشبه الألمنيوم في كثير من الخواص فيلازمه في معظم فلزاته، وهو مثله معدن مذبذب. كما أن المغنزيوم يشبه بخواصه الزنك، خاصة بسهولة انحلال كبريتاته بخلاف كبريتات الكلسيوم والسترونسيوم والباريوم. وتؤلف هذه العناصر الثلاثة الأخيرة فئة المعادن القلوية الترابية بالمفهوم الضيق لهذه التسمية التي أُطلقت عليها لتشابه خواص ماءاتها مع خواص ماءات المعادن القلوية.
وبصورة عامة يمكن تعليل تناقص الخاصة القلوية وتعاظم الخاصة الحمضية عند الانتقال من فئة المعادن القلوية إلى المعادن القلوية الترابية بتناقص أنصاف أقطار الذرات والشوارد.
إن العنصر الأخير في هذه الفصيلة هو الراديوم عنصر مشع نادر. وهو معدن قلوي ترابي بخواصه العامة، وينتج من تفكك العناصر الأثقل منه وخصوصاً اليورانيوم؛ ولذلك يصادف مع خامات اليورانيوم خاصة البتش بلند (pitch blend U3O8 غير النقي) ويعد الخام الحاوي على 0.25غ من الراديوم في الطن من الخامات الغنية.
وجودها في الطبيعة ـ استحصالها ـ خواصها الفيزيائية ـ استعمالاتها
المغنزيوم والكلسيوم المعدنان الوحيدان بين المعادن القلوية الترابية اللذان ينتشران انتشاراً واسعاً في القشرة الأرضية، فتبلغ النسبة الوزنية المئوية للمغنيزيوم 2.35%. وتوجد أملاحه في مياه المحيطات أيضاً. كما تبلغ النسبة المئوية للكلسيوم في القشرة الأرضية 25.3% وزناً. أما في حالة السترنسيوم والباريوم فتساوي هذه النسبة 0.35% و0.05% بالترتيب، وتوجد هذه العناصر الثلاثة الأخيرة في الطبيعة بشكل كربونات وكبريتات خاصة.
وكان الإنكليزي السير همفري ديڤي (1778ـ1829) Sir Humphry Davy أول من عزل المغنزيوم بطريقة التحليل الكهربائي بكميات صغيرة وأطلق عليه اسم مغْنيوم magnium وذلك حتى لايحصل التباس بينه وبين المنغنيز، إلا أن اسمه بقي مغنزيوم. كما عزل ديڤي الكلسيوم والسترنسيوم والباريوم بالطريقة نفسها عام 1808.
يحصل على عناصر هذه الفصيلة بالحالة المعدنية الحرة بتحليل أملاحها المصهورة تحليلاً كهربائياً.
|
||||||||||||||||||||||||||||||||||||||||||||
| الجدول (1) الصفات الفيزيائية للكلسيوم والسترنسيوم والباريوم |
ويبين الجدول (1) بعض الثوابت الفيزيائية لعناصر الكلسيوم والسترنسيوم والباريوم. ويلاحظ من هذا الجدول أن كهرجابية المعادن القلوية الترابية تماثل تقريباً كهرجابية المعادن القلوية، ويلاحظ أن تغير الكمون النظامي يتفق مع تغير طاقة التشرد.
أما من حيث استعمالات عناصر هذه الفصيلة فإن المغنزيوم هو المعدن الوحيد الذي يستعمل بالحالة الحرة بصورة واسعة لتحضير المواد النارية بسبب الضوء الشديد المتولد عن احتراقه، ويدخل البريليوم والمغنزيوم والكلسيوم مع المعادن الأخرى في تركيب كثير من الخلائط المعدنية فتكسبها قساوة عظيمة.
وتستعمل مركبات عناصر هذه الفصيلة في الصناعة، خاصة مركبات الكلسيوم والمغنزيوم في صناعة الإسمنت والزجاج وبعض المواد الأخرى كالأميانت والتلك. وللمغنزيوم أهمية خاصة في التحضيرات العضوية (تفاعل غرينيار).
الصفات الكيمياوية للكلسيوم والسترنسيوم والباريوم
تتصف عناصر هذه الفصيلة بكهرجابية عالية وبنشاط كيمياوي كبير كالمعادن القلوية. فمن الناحية المبدئية تفكك هذه العناصر الماء والحموض بانطلاق الهدروجين، وتشكل مركبات شاردية مع العناصر الكهرسلبية مع ازدياد بروز هذه الخواص عند الانتقال من البريليوم حتى الباريوم ومن العناصر الأقل كهرسلبية إلى العناصر الأكثر كهرسلبية.
أهم المركبات
ـ الهاليدات: تنتج من التفاعل مع الهالوجينات مركبات بلورية لا لون لها صيغتها العامة MX2 تتبلور مع الماء فتضم 6جزيئات في حالة الكلسيوم والسترنسيوم (MX2.6H2O) وجزيئين في حالة الباريوم. كما تكون هذه البلورات جيدة الانحلال في الماء، ويستثنى من ذلك الفلوريدات التي تكون صعبة الانحلال، ولاتشكل بلورات مميهة بصورة عامة.
أهم الهاليدات من الوجهة العملية كلوريد الكلسيوم: ويستعمل كلوريد الكلسيوم اللامائي مجفِّفاً، كما أن محاليله المائية تستعمل في المختبرات حمامات مائية ذات درجات غليان أو درجات تجمد مختلفة حسب تركيز الكلوريد. فتتدرج درجة الغليان من 101 ْس حتى 178 ْس وتتدرج درجة التجمد من -0.05 ْس حتى -51 ْس.
ـ الأكاسيد والماءات: يتم تفاعل المعادن القلوية الترابية مع الأكسجين في الدرجة العادية من الحرارة فتتغطى هذه المعادن في الهواء بطبقة من الأكسيد MO. غير أن هذه الطبقة تكون كتيمة في حالة المغنزيوم فتمنع استمرار التفاعل. وينشط التفاعل بشدة بتسخين المعدن ويتشكل إضافة إلى الأكسيد MO النتريد M3N2 وفوق الأكسيد MO2 في حالة Ba¨Sr¨Ca.
وتتصف الأكاسيد MO بخواص أساسية باستثناء أكسيد البريليوم الذي يتميز بخواص أساسية وحمضية (أكسيد مذبذب).
والأكاسيد MO مواد بيضاء صعبة الانصهار تتفاعل مع الماء مشكلة الماءات M(OH)2. وتزداد درجة انحلال الماءات وتشردها في الماء عند الانتقال من البريليوم حتى الباريوم، فتكون ماءات البريلوم ماءات مذبذية، في حين تكون ماءات المغنزيوم أساساً متوسط القوة، وماءات الباريوم أساساً قوياً نوعاً ما. أكسيد الكلسيوم وهو الكلس الحي ذو استعمالات معروفة.
ـ فوق الأكاسيد والأكاسيد العليا: تشكل المعادن القلوية الترابية مثل المعادن القلوية فوق أكاسيد وأكاسيد عليا. ويحصل على فوق الأكاسيد MO2 إما بالطريقة الرطبة بتفاعل الماء الأكسجيني H2O2 مع ماءات المعدن، وهو تفاعل تعديل حمض (H2O2) بأساس، كما في حالة الكلسيوم إذ يحصل على فوق أكسيده بالتفاعل:
 |
وتكون فوق الأكاسيد مواد بيضاء، تحوي في بنيتها الشاردة
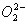 وتعطي بتفاعلها مع الحموض الماء الأكسجيني والملح الموافق للمعدن. أهمها من الوجهة التطبيقية فوق أكسيد الباريوم الذي يستخدم صناعياً للحصول على الماء الأكسجيني بتفاعله مع حمض الكبريت وفق المعادلة:
وتعطي بتفاعلها مع الحموض الماء الأكسجيني والملح الموافق للمعدن. أهمها من الوجهة التطبيقية فوق أكسيد الباريوم الذي يستخدم صناعياً للحصول على الماء الأكسجيني بتفاعله مع حمض الكبريت وفق المعادلة:  |
ـ الكربيدات: لايتم تفاعل المعادن القلوية الترابية مع الكربون سوى في درجة عالية من الحرارة أيضاً وتتشكل الكربيدات. وهي تتصف بصورة عامة ببنية شاردية خاصة في حالة الكلسيوم والسترنسيوم والباريوم التي تعطي الكربيد MC2
الذي يحوي الشاردة الخطية السالبة
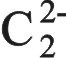 .
.أهم الكربيدات كربيد الكلسيوم الذي يعرف في التجارة باسم الكربيد، ويستعمل لتوليد غاز الأستيلين
 |
 |
 |
 |
شوارد المعادن القلوية الترابية لا لون لها، وأملاحها لا لون لها أيضاً بصورة عامة. منها ما ينحل جيداً في الماء كأملاح الشوارد:
 ومنها ما يكون صعب الانحلال لا في الماء فحسب، بل في المحلات الأخرى، كأملاح الشوارد
ومنها ما يكون صعب الانحلال لا في الماء فحسب، بل في المحلات الأخرى، كأملاح الشوارد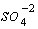 و
و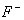 و
و و
و و
و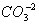 . ولكثير من هذه الأملاح تطبيقات مهمة في الصناعة وسيكتفى بدارسة بعض هذه الأملاح كالكبريتات والنترات والكربونات.
. ولكثير من هذه الأملاح تطبيقات مهمة في الصناعة وسيكتفى بدارسة بعض هذه الأملاح كالكبريتات والنترات والكربونات.الكبريتات MSO4: تتبلور كبريتات المغنزيوم والكلسيوم مع عدد مختلف من جزيئات الماء فتكون صيغها:
BeSO4. 4H2O¨CaSO4. 2H2O¨MgSO4. 7H2O
أما كبريتات السترنسيوم والباريوم فلا تحوي بلوراتها ماء تبلور. وتتناقص درجة الانحلال في الماء عند الانتقال من البريليوم حتى الباريوم. فكبريتات البريليوم والمغنزيوم جيدة الانحلال، أما كبريتات الباريوم فهي ملح صعب الانحلال. ويقل الانحلال بارتفاع درجة الحرارة.
وأهم أملاح الكبريتات كبريتات الباريوم المستعملة في الطب، وكبريتات الكلسيوم التي تتبلور في الدرجة العادية من الحرارة مع جزيئي ماء، وتشكل ما يعرف باسم «الجبصين». إذا سخنت هذه الكبريتات إلى درجة 150 ْس فقدت قسماً من مائها وتحولت إلى 2CaSO4.H2O. وعند مزج هذه المادة الأخيرة بالماء تتحد مرة أخرى مع الماء لتكوين البلورات المميهة مما يؤدي إلى تصلب المزيج مع ازدياد حجمه، ويستفاد من ذلك لصب القوالب كما هو معروف.
النترات M(NO3)2: تتبلور نترات المعادن القلوية الترابية مع عدد من جزيئات الماء باستثناء نترات الباريوم، وصيغها:
Mg(NO3)2.6H2O, Ca(NO3)2.4H2O, Sr(NO3)2.4H2O
وهي تنحل جيداً في الماء باستثناء نترات الباريوم أيضاً التي تكون متوسطة الانحلال. تتفكك النترات بالتسخين فاقدة في مرحلة أولى ماء التبلور ومن ثم تتحول إلى أكاسيد الآزوت والأكاسيد MO وأكسجين.
الكربونات MCO3: الكربونات المعتدلة MCO3 عديمة الانحلال في الماء. وهي تتفكك بالتسخين حيث ينطلق CO2 ويتشكل الأكسيد MO. وتترسب الكربونات بإضافة مزيد من الشوارد

إلى محلول يحوي الشوارد M2+x.
وأهم الكربونات ـ من الناحية العملية ـ كربونات الكلسيوم. وتستخدم بمختلف أشكالها الطبيعية (الأحجار الكلسية) للحصول على الكلس والإسمنت وفي صناعة الزجاج.
فالإسمنت مزيج من مختلف سيلكات وألومينات الكلسيوم وبالدرجة الأولى المركبات: Ca2SiO5, Ca2SiO4, Ca3(AlO3)2. فيعد الإسمنت ناتج اتحاد مختلف الأكاسيد الآتية بنسب مختلفة: CaO, SiO2, Al2O3, Fe2O3 حيث يقوم الأكسيد CaO بدور الأكسيد الأساسي في حين تقوم الأكاسيد الأخرى بدور الأكاسيد الحمضية.
وتتفاعل الكربونات MCO3 مع ثنائي أكسيد الكربون المنحل في الماء مكونة الكربونات الحمضية M(HCO3)2 الأكثر انحلالاً من الكربونات، أهمها كربونات الكلسيوم الحمضية Ca(HCO3)2.
يسبب وجود أملاح الكلسيوم في الماء قساوته. وتكون هذه القساوة مؤقتة عندما يحوي الماء الكربونات الحمضية Ca(HCO3)2 وذلك لسهولة إزالة هذه القساوة بترسيب الكلسيوم بشكل CaCO3 بغلي الماء إذ تتفكك الكربونات الحمضية إلى كربونات معتدلة و CO2. وتكون القساوة دائمة عندما يكون الملح المنحل CaSO4 أو CaCl2. وتُزال هذه القساوة إما بإضافة Na2CO3 لترسيب CaCO3، وإما بالتبادل الشاردي الذي يخلص الماء من شوارد الكلسيوم، وإما بالتقطير.
غدير زيزفون
